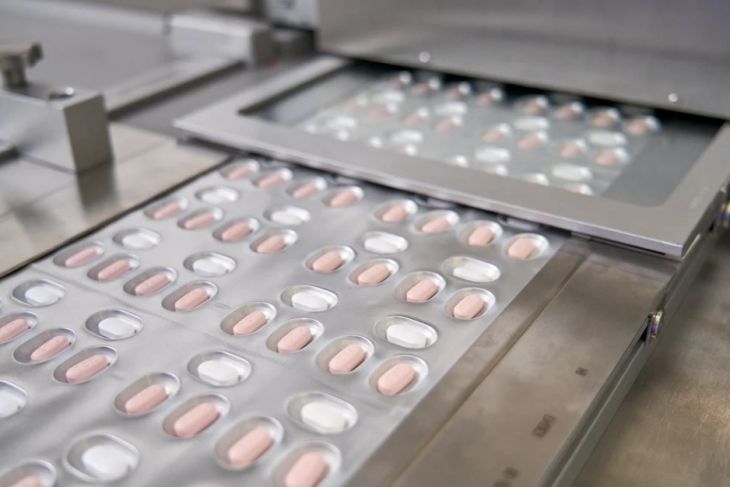
El regulador de medicamentos de la Unión Europea aprobó este jueves la píldora de Pfizer contra el Covid-19 para su uso de emergencia por parte de los Estados miembros individuales que luchan contra la nueva ola de la enfermedad, a la espera de la aprobación formal en todo el bloque.
El martes, la empresa estadounidense anunció los resultados finales de su estudio de Fase II/III, basados en un análisis de 2 mil 246 voluntarios, y reportó que el fármaco antiviral, denominado Paxlovid, redujo la hospitalización o la muerte entre las personas de alto riesgo en 89 por ciento.
Lee: Pfizer: Pastilla contra Covid-19 tiene 89 por ciento de efectividad
“El medicamento, que aún no está autorizado en la UE, puede utilizarse para tratar a los adultos con Covid-19 que no requieren oxígeno suplementario y que tienen un mayor riesgo de progresar a la enfermedad grave”, dijo la Agencia Europea de Medicamentos en un comunicado.
“La EMA ha emitido este consejo para apoyar a las autoridades nacionales que puedan decidir sobre el posible uso temprano del medicamento... por ejemplo, en contextos de uso de emergencia, a la luz de las crecientes tasas de infección y muertes debidas a Covid-19 en toda la UE.”
Este jueves, la EMA también anunció la autorización del anticuerpo monoclonal sotrovimab desarrollado por GlaxoSmithKline y Vir Biotechnology; y Kineret, de la compañía sueca Sobi, un medicamento inmunosupresor que ya tenía autorización de la UE para tratar enfermedades inflamatorias.
El tratamiento de Pfizer, denominado Paxlovid, es una combinación de una nueva molécula, PF-07321332, y el antiviral contra el VIH ritonavir, que se toman en comprimidos separados.
También te puede interesar: Pfizer, menos eficaz contra hospitalización por ómicron: estudio
“Paxlovid debe administrarse lo antes posible tras el diagnóstico de Covid-19 y dentro de los cinco días siguientes al inicio de los síntomas”, señaló la EMA, añadiendo que los comprimidos deben tomarse después durante cinco días más.
Los efectos secundarios más comunes fueron una alteración del sentido del gusto, diarrea y vómitos. El fármaco no debe ser utilizado por mujeres embarazadas, y la lactancia debe interrumpirse mientras se esté tomando, añadió.
El organismo de control, con sede en Ámsterdam, dijo que al mismo tiempo estaba iniciando una “revisión continua” de la píldora de Pfizer que podría conducir a su eventual aprobación en cuestión de meses.
La EMA ya ha emitido una aprobación de uso de emergencia similar para una píldora del rival de Pfizer, Merck.
Edición: Emilio Gómez
Es necesario consolidar en modelo que priorice la sustentabilidad y la justicia ecológica
Óscar Alberto Rébora Aguilera
Tres décadas de negligencia y dos administraciones de un gobierno que prefiere mirar a otro lado
Juan Carlos Pérez Castañeda