Unos robots microscópicos hechos a base de células de algas pueden introducirse en el cuerpo y nadar alrededor de los pulmones para administrar medicación y eliminar casos de neumonía bacteriana, según una prueba hecha en ratones.
Los microrobots eliminaron de los pulmones de ratones, de forma segura, una bacteria que causa neumonía y se logró un 100 por ciento de supervivencia. Por el contrario, los roedores que no recibieron el tratamiento murieron a los tres días de la infección.
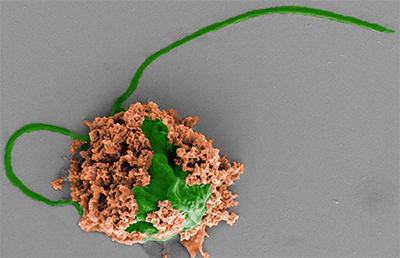
Los pequeños robots están formados por células de algas cuya superficie está salpicada de nanopartículas llenas de antibióticos, indica el estudio, que publica en Nature Materials y está encabezado por la Universidad de California San Diego.
Las algas aportan movimiento, lo que permite a los microrobots nadar y administrar los antibióticos directamente a más bacterias en los pulmones.
Las nanopartículas que contienen el antibiótico están fabricadas con pequeñas esferas de polímero biodegradable y cubiertas con membranas celulares de neutrofilos, que son un tipo de célula sanguínea
Lo especial de estas membranas celulares es que absorben y neutralizan las moléculas inflamatorias producidas por las bacterias y el sistema inmunitario del organismo, lo que da a los microrobots la capacidad de reducir la inflamación perjudicial, lo que a su vez los hace más eficaces para combatir la infección pulmonar.
El equipo usó los microrobots para tratar a ratones de una forma aguda y potencialmente mortal de neumonía causada por la bacteria Pseudomonas aeruginosa, que es la que normalmente afecta a los pacientes sometidos a ventilación mecánica en las unidades de cuidados intensivos.
Los investigadores administraron los microrobots en los pulmones de los ratones a través de un tubo insertado en la tráquea y la infección desapareció totalmente tras una semana.
Además, fue más eficaz que la administración de antibióticos en el torrente sanguíneo con una inyección, la cual requiere una dosis 3 mil veces mayor para lograr el mismo efecto que con la nueva técnica.
"Estos resultados muestran cómo la administración selectiva de fármacos, combinada con el movimiento activo de las microalgas, mejora la eficacia terapéutica", dijo Joseph Wang, uno de los firmantes del estudio.
Una vez completado el tratamiento, el sistema inmunitario del cuerpo elimina de manera eficaz las algas y muchas de las nanopartículas que quedan. “No queda nada tóxico”, agregó.
El trabajo es una prueba de concepto y el equipo tiene previsto seguir con más investigación básica para entender exactamente cómo los microrobots interactúan con el sistema inmunitario, además de validar el tratamiento antes de probarlo en animales más grandes y, eventualmente, en personas.
El equipo ya ha desarrollado otros dispositivos diminutos dispensadores de fármacos, que pueden utilizarse en animales para tratar infecciones bacterianas en el estómago y la sangre.
El objetivo con este estudio -señaló el investigador- era administrar fármacos de forma selectiva en partes del cuerpo más difíciles, como los pulmones, y hacerlo de forma segura, fácil, biocompatible y duradera.
Nota relacionada: Detectan neumonía de forma automática con inteligencia artificial
Edición Astrid Sánchez
Gobierno federal, estado y comunidades impulsarán un decreto para proteger la zona y promover el desarrollo sustentable
Rosario Ruiz Canduriz
Microorganismos ancestrales y modernos conviven desde hace más de 5 mil años en el cuerpo del Hombre de Hielo
Efe
Infraestructura, salud, agua, carreteras y desarrollo social concentran el mayor paquete de inversión federal para el estado
La Jornada
España empata con Irak y Chequia, rival de México, supera 3-1 a Guatemala
Ap