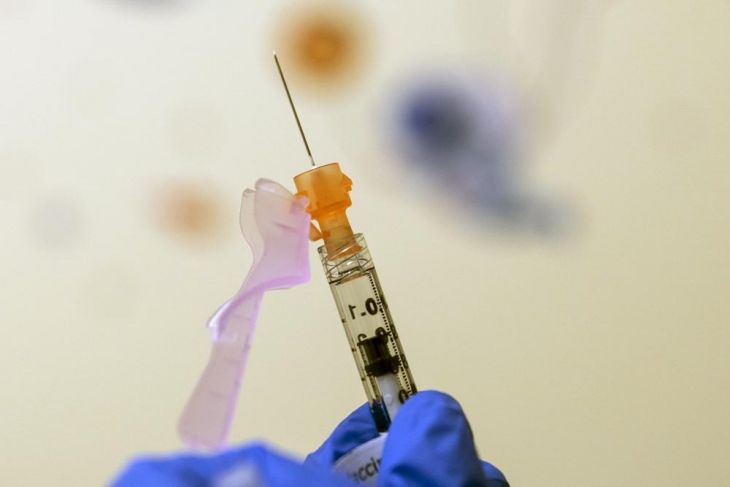
Pfizer solicitó el martes al gobierno de Estados Unidos que autorice el uso de su vacuna contra el Covid-19 en dosis muy bajas para niños menores de cinco años, lo que allanaría el camino para que los estadunidenses más jóvenes empiecen a recibir la vacuna a partir de marzo.
En una medida extraordinaria, la Administración de Alimentos y Medicamentos (FDA, por sus siglas en inglés) les había pedido a Pfizer y a su socio BioNTech que presentaran la solicitud de autorización antes de lo que las compañías tenían contemplado.
Los 19 millones de niños menores de cinco años en Estados Unidos son el único grupo que todavía no es elegible a recibir la vacuna contra el Covid-19. Muchos padres de familia han estado presionando porque se expanda la campaña de vacunación e incluya a bebés y niños en edad prescolar, en particular en momentos en que la oleada de la variante ómicron deja cifras récord de hospitalizaciones entre los menores.
También te puede interesar: Pfizer inicia estudio de vacuna actualizada contra ómicron
Si la FDA da su autorización, inyecciones de la vacuna de Pfizer con una décima parte de la dosis que se administra a los adultos, podrían empezarse a aplicar en niños de hasta seis meses de edad. Pfizer dijo el martes que había empezado a entregar su información a la FDA y que espera completar el proceso en pocos días.
Sin embargo, una cuestión pendiente es cuántas dosis necesitarán los pequeños. Pfizer realiza pruebas con un esquema de tres inyecciones una vez que las dos aplicaciones de la dosis en cantidades bajas resultaron lo suficientemente fuertes para los bebés, pero no para los niños en edad prescolar, y no se tiene previsto que los datos finales estén listos hasta finales de marzo.
Eso significa que la FDA podría considerar autorizar las dos dosis por ahora, con la posibilidad de que se apruebe una tercera si el estudio lo respalda.
La FDA dijo el martes que convocará a un panel de investigadores y médicos independientes a mediados de febrero para revisar los datos presentados por Pfizer. La agencia no está obligada a seguir las recomendaciones del panel, pero su aportación es un paso clave en la examinación pública de la seguridad y efectividad de las vacunas.
La decisión final de la FDA podría emitirse dentro de un mes, pero ese no es el único obstáculo. Los Centros para el Control y la Prevención de Enfermedades (CDC por sus siglas en inglés) también tienen que dar su visto bueno.
El gobierno del presidente Joe Biden ha tratado de acelerar el proceso de autorización de las vacunas contra el Covid-19 para los niños, señalando que la inmunización es esencial para poder reabrir las escuelas y guarderías y mantenerlas en operaciones, y para liberar a los padres de las labores del cuidado de los niños para que puedan volver al trabajo.
Sigue leyendo:
-90 millones de casos de Covid-19 desde llegada de ómicron: OMS
-OMS recomienda extender uso de vacuna Pfizer a niños de 5 a 11 años
-Refuerzo de Pfizer y Moderna, protección de 90 por ciento contra hospitalización: CDC
Edición: Estefanía Cardeña
La empresa de Elon Musk buscaría recaudar 75 mil mdd en lo que podría convertirse en la mayor OPI de la historia
Reuters
El municipio contará con dos nosocomios renovados para brindar atención a las y los yucatecos
Astrid Sánchez
Alcaldesa Cecilia Patrón encabezó el festejo que fortalece el tejido social
La Jornada Maya
Reitera Rusia su apoyo a Cuba frente a situación ''verdaderamente difícil''
La Jornada